医疗器械不良事件监测和再评价管理办法施行日期,不良事件监测与再评价管理办法
医疗器械不良事件监测和再评价管理办法施行日期解读
1.1 《办法》的发布背景与实施时间
- 医疗器械作为保障公众健康的重要工具,其安全性始终是监管的核心。随着技术发展和产品种类增多,不良事件的发生频率也在上升。
- 国家市场监督管理总局和国家卫生健康委员会联合发布了《医疗器械不良事件监测和再评价管理办法》,这是中国在这一领域的重要制度性文件。
- 该办法自2019年1月1日起正式施行,标志着我国在医疗器械安全监管方面迈出了关键一步。
- 此前的相关规定多为规范性文件,而《办法》首次以部门规章形式出现,提升了法律层级,增强了执行力度。
- 实施日期的设定,体现了政策制定者对行业适应性和监管落地的充分考量。
1.2 实施日期对行业的影响分析
- 自2019年1月1日施行以来,《办法》迅速成为医疗器械企业必须遵守的重要法规。
- 企业开始重新审视自身的不良事件监测流程,确保符合新规定的要求。
- 监管机构也同步加强了对企业的监督检查,推动行业整体合规水平提升。
- 实施日期的确定,让企业有足够的时间进行内部调整和系统升级。
- 这一时间节点的设定,不仅有助于政策平稳过渡,也为后续监管提供了明确依据。
1.3 与以往政策的对比与改进之处
- 与之前的政策相比,《办法》在责任划分上更加清晰,尤其是明确了上市许可持有人的主体责任。
- 原有的制度更多依赖于鼓励机制,而《办法》则引入了更严格的法律责任条款。
- 在风险控制方面,《办法》提出了更具操作性的措施,帮助企业及时发现并处理潜在问题。
- 再评价机制的完善,使得医疗器械的安全性评估更加系统化、科学化。
- 整体来看,《办法》在制度设计上更加注重实效,强化了监管与企业的双向责任。
不良事件监测与再评价管理办法实施要点解析
2.1 《办法》的核心内容与制度创新
- 《医疗器械不良事件监测和再评价管理办法》首次以部门规章形式出现,提升了法律地位,增强了执行效力。
- 办法共九章八十条,覆盖了从总则到法律责任的全过程,为行业提供了全面的操作指南。
- 核心内容聚焦于不良事件的报告、分析、风险控制以及再评价机制,确保医疗器械在使用过程中的安全性。
- 制度创新体现在对上市许可持有人的责任强化、监管流程的规范化以及信息共享机制的建立。
- 这一系列改革举措,标志着我国在医疗器械监管领域迈入了更加精细化、系统化的阶段。
2.2 上市许可持有人的责任强化
- 《办法》明确要求上市许可持有人承担不良事件监测和再评价的主要责任,确保产品全生命周期的安全管理。
- 持有人需建立完善的监测体系,及时收集、分析并上报不良事件信息,形成闭环管理。
- 责任细化后,企业必须投入更多资源用于数据管理和风险评估,提升内部合规能力。
- 对未履行责任的企业,《办法》设定了明确的处罚措施,增强制度约束力。
- 这一变化推动企业从被动应对转向主动管理,从根本上提升产品质量和用户信任度。
2.3 监管机制与法律责任的明确
- 《办法》建立了多层次的监管机制,涵盖日常检查、专项督查和飞行检查等多种形式。
- 监管机构有权根据不良事件情况采取风险控制措施,包括暂停销售、召回等手段。
- 法律责任部分明确了不同情形下的处罚标准,包括警告、罚款、吊销资质等。
- 违法行为的界定更加清晰,避免了执法过程中的模糊地带,提高了监管透明度。
- 明确的监管与法律责任体系,不仅规范了企业行为,也为公众用械安全提供了坚实保障。
医疗器械不良事件监测体系的构建与完善
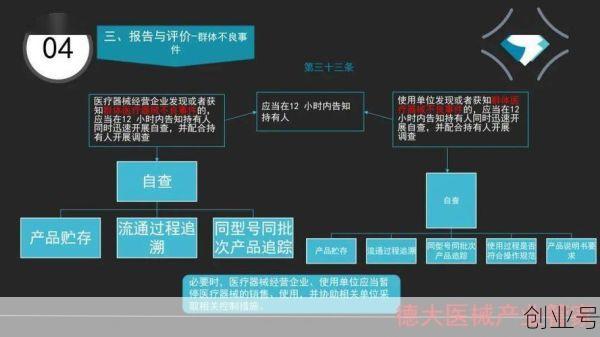
3.1 不良事件报告与评价流程详解
- 医疗器械不良事件的报告流程是整个监测体系的基础环节,涉及信息收集、分类、分析和上报等多个步骤。
- 企业需建立标准化的报告机制,确保在发现不良事件后第一时间进行记录和评估。
- 报告内容应包括产品名称、使用情况、事件描述、可能原因等关键信息,为后续分析提供依据。
- 评价流程则由专业机构或监管部门主导,通过对数据的深入分析,判断事件是否属于医疗器械本身的问题。
- 完善的报告与评价机制能够快速识别潜在风险,为后续风险控制和再评价提供有力支撑。
3.2 风险控制措施与应对策略
- 针对已确认的不良事件,企业需立即启动风险控制程序,防止问题进一步扩大。
- 常见的风险控制措施包括暂停销售、召回产品、修改说明书以及发布警示信息等。
- 企业应根据事件严重程度制定分级响应策略,确保应对措施科学、合理且有效。
- 同时,风险控制还应结合数据分析结果,持续优化产品设计和使用规范。
- 灵活而高效的应对策略,不仅有助于减少损失,还能提升企业的社会责任感和市场信誉。
3.3 再评价机制在医疗器械安全中的作用
- 再评价是医疗器械不良事件监测体系的重要组成部分,旨在通过持续评估确保产品安全性。
- 当发现新的风险信号或长期使用中暴露问题时,企业必须启动再评价程序。
- 再评价过程需要收集大量临床数据,并结合专家意见进行综合分析,形成改进建议。
- 这一机制能够推动企业不断改进产品性能,提高整体医疗质量。
- 再评价不仅是监管要求,更是保障公众健康、提升行业水平的关键手段。
《办法》实施后的行业影响与未来展望
4.1 对医疗器械企业的影响与挑战
- 《办法》的正式施行,让医疗器械企业面临更严格的监管要求,尤其是对不良事件的报告和再评价流程提出了更高标准。
- 企业需要重新审视自身的质量管理体系,确保在产品上市后能够持续监测并及时响应潜在风险。
- 不良事件报告的责任主体明确为上市许可持有人,这促使企业加大内部合规投入,提升专业能力。
- 面对日益复杂的数据分析和风险评估任务,企业需建立专门团队或引入第三方机构协助完成相关工作。
- 虽然短期内增加了运营成本,但从长远来看,这种规范化的管理有助于增强企业的市场竞争力和品牌信任度。
4.2 公众用械安全的保障与提升
- 《办法》的实施直接关系到公众用械安全,通过强化监测和再评价机制,有效降低因产品缺陷引发的健康风险。
- 消费者在使用医疗器械时,能获得更多透明的信息,包括产品风险提示、使用建议和更新动态。
- 一旦发生不良事件,监管部门能够更快介入,减少对患者健康的负面影响。
- 公众对医疗器械的信任度随之提升,推动整个行业向更高质量方向发展。
- 更加完善的制度保障,让医疗设备成为真正值得信赖的健康工具,惠及更多人群。
4.3 未来监管趋势与政策发展方向
- 随着《办法》的深入实施,未来监管将更加注重数据驱动和智能化管理,推动信息化平台建设。
- 监管部门可能会进一步细化责任划分,加强对企业合规行为的监督检查力度。
- 政策层面或将出台配套措施,如鼓励企业开展主动风险评估、支持创新产品快速审批等。
- 行业标准和操作指南也将不断完善,为企业提供更清晰的执行路径和参考依据。
- 未来医疗器械监管将朝着更科学、更高效、更人性化的方向发展,持续提升我国医疗设备的安全水平。
(医疗器械不良事件监测和再评价管理办法施行日期,不良事件监测与再评价管理办法)
本文系作者个人观点,不代表本站立场,转载请注明出处!